辉瑞新冠口服特效药获准进入中国
辉瑞新冠口服特效药获准进入中国,这为口服小分子新冠病毒治疗药物,国内上市的第一款口服新冠药物,也是迄今为止国内上市的第二款新冠治疗药物。辉瑞新冠口服特效药获准进入中国。
辉瑞新冠口服特效药获准进入中国1
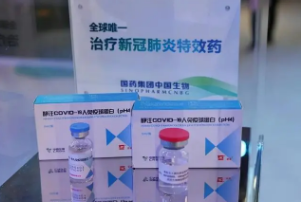
新冠口服特效药获准进入中国。2月11日,国家药监局批准辉瑞新冠病毒治疗药物奈玛特韦片/利托那韦片组合包装(即Paxlovid)进口注册,本品为口服小分子新冠病毒治疗药物,用于治疗成人伴有进展为重症高风险因素的轻至中度新型冠状病毒肺炎(COVID-19)患者。相比于大分子药物(如注射用中和抗体药物等),小分子口服药具有抗病毒效果直接、生产成本和用药成本低、运输和储运条件易满足、居家服用方便等优势,因此被寄予终结疫情的厚望。
叠加有序放开预期持续验证。国家应急防控药物工程技术研究中心研究员钟武表示:“目前感染新冠病毒的患者中,轻中症患者占到85%以上,这些人如果能居家就用上小分子口服药物进行治疗的话,不仅可以快速消灭病毒,还可以将传染给其他人的风险降到最低,同时可以缩短隔离的时间,对改变我国现有的疫情防控策略可能会发挥重要作用。”因此,我们可以合理预期,新冠口服特效药Paxlovid进口到中国后,将加速推动我国疫情防控政策的调整,政策有序放开和实体景气修复的预期将进一步显著增强。
基于整体消费板块政策加持预期增强,看好酒旅餐饮板块投资机会。目前来看,国内外疫情放宽趋势正在持续得到验证,如开放国门、试行恢复直航等先后出台。1)2月7日下午,澳大利亚总理官宣:澳大利亚将于2月21日向剩余签证持有者重新开放国际边界,入境者需持有效签证+已接种2剂受认可的疫苗即可入境。在美英等国去年下半年已逐步开放国门的背景下,澳大利亚曾被戏称“隐士国家”,我们认为此举意味国际旅行市场整体趋势向好。2)2月9日,来自英国工业联合会CBI的消息,中国和英国之间可能在本月展开为期两周的直航复航测试,如果测试成功可能在未来恢复中英两国之间的定期直飞航线。计划测试将在本月中下旬开始,航线为两条从伦敦希思罗LHR-上海浦东PVG的往返航线,最大载客人数为30%。3)2月9日,云南省文旅厅官宣"关于我省即日起恢复跨省团队旅游的通知",鉴于目前云南省已无疫情防控中高风险地区,自2022年2月9日起,恢复云南省旅行社及在线旅游企业经营跨省团队旅游及“机票+酒店”业务。
辉瑞新冠口服特效药获准进入中国2
2月11日,国家药监局附条件批准了美国辉瑞公司新冠病毒治疗药物奈玛特韦片/利托那韦片组合包装(即Paxlovid)进口注册。这是国内上市的第一款口服新冠药物,也是迄今为止国内上市的第二款新冠治疗药物。
2021年12月8日,国家药品监督管理局应急批准腾盛华创医药技术(北京)有限公司新冠病毒中和抗体联合治疗药物安巴韦单抗注射液(BRII-196)及罗米司韦单抗注射液(BRII-198)注册申请。
国内患者何时能用上新冠特效药呢?2月14日,健康时报记者分别联系了辉瑞和腾盛博药。
国内第一个口服新冠药物:上市消息将及时公布
据国家药监局介绍,Paxlovid为口服小分子新冠病毒治疗药物,用于治疗成人伴有进展为重症高风险因素的轻至中度新型冠状病毒肺炎(COVID-19)患者,例如伴有高龄、慢性肾脏疾病、糖尿病、心血管疾病、慢性肺病等重症高风险因素的患者。
2月14日,健康时报记者从辉瑞公司获悉,目前Paxlovid刚刚获批,具体的上市计划尚不掌握,若想知道药品何时上市、在什么城市的哪些医院落地等信息,还需等待一些时日。有消息将第一时间公布。
图片源自新华社。
根据美国食品药品监督管理局(FDA)的提示,Paxlovid由奈玛特韦片(nirmatrelvir)和利托那韦片(ritonavir)组成,奈玛特韦片可以抑制SARS-CoV-2蛋白的复制,而利托那韦片可以减缓奈玛特韦片的分解,帮助药物在更高浓度下更长时间地留在体内。治疗时服用三片药,即两片奈玛特韦片和一片利托那韦片,每天口服两次,持续5天,且不能连续使用超过5天。
美国食品药品监督管理局在一份声明中强调,对于那些建议接种新冠病毒疫苗和加强剂量的个人来说,Paxlovid不能替代疫苗接种。
临床试验数显示,与安慰剂相比,在症状出现的三天内(主要终点),接受Paxlovid治疗的成人与COVID-19相关的住院或因任何原因死亡的风险降低了89%。在症状出现后5天内接受治疗的患者(次要终点)中,住院或因任何原因死亡的风险降低了88%,并且在治疗组中没有观察到死亡。
国内首款新冠单克隆中和抗体:正在推进生产供应事宜
2021年12月8日,国家药品监督管理局应急批准腾盛华创医药技术(北京)有限公司新冠病毒中和抗体联合治疗药物安巴韦单抗注射液(BRII-196)及罗米司韦单抗注射液(BRII-198)注册申请,批准上述两个药品联合用于治疗轻型和普通型且伴有进展为重型(包括住院或死亡)高风险因素的成人和青少年(12―17岁,体重≥40kg)新型冠状病毒感染(COVID-19)患者。其中,青少年(12―17岁,体重≥40kg)适应症人群为附条件批准。
2月14日,健康时报记者从腾盛华创获悉,该公司正积极推进生产及供应工作,以尽早实现药物上市,以惠及新冠患者。
安巴韦单抗和罗米司韦单抗是我国首家获批的自主知识产权新冠病毒中和抗体联合治疗药物,由清华大学、深圳市第三人民医院及腾盛博药生物科技公司合作研发。

企业供图。
2021年12月4日,腾盛华创获得了三期临床试验全部受试者的数据。最终结果显示,与安慰剂相比,该联合疗法使临床为高风险的新冠门诊患者住院和死亡风险降低80%,并且药品临床安全性优于安慰剂组。目前的体外嵌合病毒实验检测数据表明,该联合疗法对奥密克戎、德尔塔、德尔塔+、阿尔法、贝塔、伽马、拉姆达等新冠病毒变异株均保持了中和活性。
清华大学医学院教授张林琦在产品发布会上表示,无论早期即开始接受治疗(症状出现后5天内)还是晚期才开始接受治疗(症状出现后6至10天内)的受试者,住院和死亡率均显著降低,这为新冠患者提供了更长的治疗窗口期。
据腾盛博药提供的信息,新冠病毒主要通过与人体细胞上的ACE2结合感染人体细胞,并通过细胞繁殖造成疾病。安巴韦单抗针对新冠病毒受体结合区域与ACE2直接结合的部位,阻断病毒与ACE2结合。而罗米司韦单抗针对新冠病毒受体结合区域另一个不与ACE2结合的位点,以不同作用机制阻断病毒的繁殖。据悉,该中和抗体联合疗法采用静脉注射的方式,一次注射时间约1小时左右,只需一次给药即完成治疗。
此外,钟南山院士带领的广州实验室团队正在开展安巴韦单抗和罗米司韦单抗联合疗法用于预防的研究工作,推动其在疫苗反应欠佳人群中的预防使用。
辉瑞新冠口服特效药获准进入中国3
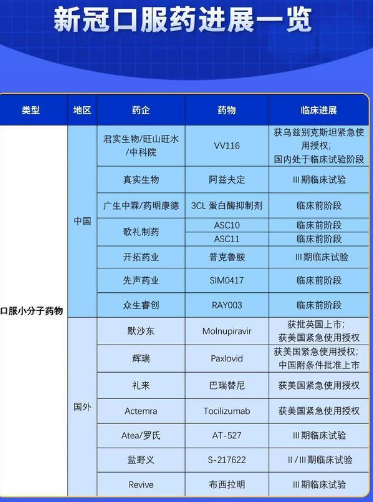
2月12日,国家药监局发布公告,按照药品特别审批程序,进行应急审评审批,附条件批准辉瑞公司新冠病毒治疗药物奈玛特韦片/利托那韦片组合包装(即)进口注册。人民日报健康客户端不完全统计发现,包括辉瑞此次获批的新冠口服药在内,目前在研的新冠口服药共有15款,其中多款为“老药新用”,5款新冠口服药已获得紧急使用授权/上市批准。
辉瑞:Paxlovid住院死亡风险降低89%,多国紧急使用授权
据辉瑞微信公众号消息,Paxlovid是一款口服小分子新冠病毒治疗药物,由两片尼马瑞韦和一片利托那韦组成,尼马瑞韦可以通过抑制SARS-CoV-2蛋白来阻止病毒复制,利托那韦可以通过减缓尼马瑞韦的分解来维持药效。
于我国获批前,美国当地时间2021年12月22日,美国食品药品监督管理局(FDA)已向辉瑞的Paxlovid(由尼马瑞韦片和利托那韦片共同组成)颁发了紧急使用授权(EUA),用于12岁以上、体重40kg以上轻度至中度新冠患者,以及有发展成新冠重症(包括住院或死亡)的高风险人群。
支持Paxlovid获得美国FDA紧急使用授权批准的主要数据来自一项随机、双盲、安慰剂对照临床试验。数据表明,与安慰剂相比,在症状出现的三天内(主要终点),接受Paxlovid治疗的成人与COVID-19相关的住院或因任何原因死亡的风险降低了89%。在症状出现后5天内接受治疗的患者(次要终点)中,住院或因任何原因死亡的风险降低了88%,并且在治疗组中没有观察到死亡。
除美国以外,欧洲药品管理局(EMA)人用医药产品委员会在2021年12月16日发布建议,支持欧盟成员国在获得欧盟有条件营销授权之前,紧急使用Paxlovid。
默沙东:全球首个获批上市的新冠口服药,将住院或死亡风险降低约30%
另一款备受瞩目的新冠口服药物Molnupiravir则是“老药新用”的典型案例。早在2021年11月4日,默沙东就宣布英国药品和保健产品监管局已批准Molnupiravir在英国上市,用于治疗轻至中度COVID-19成人患者,Molnupiravir也由此成为全球首个获批上市的新冠口服药。

2021年12月23日,Molnupiravir获美国食品药品监督管理局紧急使用授权,用于治疗 SARS-CoV-2 病毒直接检测结果呈阳性的成人轻中度冠状病毒病 (COVID-19),并且有发展为严重 COVID-19 的高风险,包括住院或死亡,以及 FDA 授权的 COVID-19 替代治疗方案无法获得或临床上不合适的人。
根据III期MOVe-OUT临床试验中期分析结果,Molnupiravir可将进展为重症或死亡的风险降低了50%,且将死亡率拉低至0%。不过,根据默沙东提交给美国FDA的最终数据,该药可将未接种疫苗的'高风险人群住院或死亡风险降低约为30%。
礼来:巴瑞替尼可在标准疗法基础上将死亡风险降低38%
巴瑞替尼也是一款“老药”,此前在美国获批用于治疗中度至重度类风湿性关节炎(RA)和特应性皮炎成人患者。疫情期间,英国人工智能公司BenevolentAI通过其研发的AI平台检索海量科学文献,发现巴瑞替尼或可用于治疗新冠。
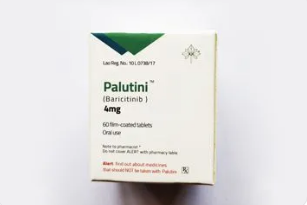
目前,巴瑞替尼已获得美国FDA紧急使用授权,用于治疗需要辅助供氧、无创或有创机械通气或体外膜肺氧合(ECMO)的2岁以上新冠患者以及与瑞德西韦联用。
2021年4月,礼来公布的一项覆盖1525名患者的临床试验数据显示,相比包括地塞 米松、瑞德西韦的标准疗法,巴瑞替尼在此基础上使新冠肺炎患者的死亡风险降低了38%。但这一试验也发现,在防止患者病程恶化至呼吸器或死亡这一目标上,巴瑞替尼没有显著效果。
君实生物:国际多中心II/III期临床试验正在进行中,已在乌兹别克斯坦获紧急使用授权
VV116是一款口服核苷类抗新冠病毒药物,由君实生物与旺山旺水合作开发。VV116与另一款新冠治疗药物瑞德西韦渊源颇深,VV116根据瑞德西韦改造而来,主要是在保持抗冠状病毒活性的前提下,通过前药策略改善其口服生物利用度。
目前,VV116已在乌兹别克斯坦获紧急使用授权。人民日报健康客户端从君实生物获悉,VV116正在开展全球多中心临床研究,其中3项在中国开展的I期研究已于近日完成,初步结果显示临床安全性良好,针对轻中度COVID-19患者的国际多中心II/III期临床试验正在进行中。年内通过临床试验后,将第一时间启动上市(NDA)申请。
临床前的药代动力学等研究结果显示,VV116具有很高的口服生物利用度,其口服吸收后,迅速代谢为母体核苷,并在体内组织广泛分布。VV116在体外对SARS-CoV-2原始株和已知突变株都表现出显著的抗病毒作用。在小鼠模型上,低剂量的VV116即可将肺部病毒滴度降低至检测限以下,可显著改善肺组织病理变化,表现出较强的抗病毒功效。
开拓药业:Ⅲ期临床试验已完成中国首例受试者入组及给药
普克鲁胺为开拓药业开发的新冠口服小分子药,据开拓药业公告,2月10日,开普克鲁胺治疗轻中症新冠患者全球多中心Ⅲ期临床试验已在深圳市第三人民医院完成中国首例受试者入组及给药。
此前, 2021年12月27日,开拓药业曾发布公告称普克鲁胺在全球III期临床试验中未达到统计学显著性,开拓药业预计调整临床试验设计,继续招募只有基础性疾病和/或无新冠疫苗接种史的高风险新冠患者。
与其他药物不同,公开资料显示,普克鲁胺最早是开拓药业拟用于治疗前列腺癌和乳腺 癌的一款药物。经系列研究后发现,普克鲁胺可以通过下调新冠病毒入侵宿主细胞的两个关键蛋白的表达水平,阻止新冠病毒入侵宿主细胞,对新冠感染早期和中后期也有很好的疗效。
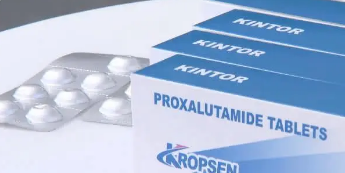
普克鲁胺在海外Ⅲ期临床试验中的数据相当亮眼。开拓药业资料显示,普克鲁胺预防轻症转为重症的住院保护率,男女分别为92%和90%,ICU或死亡保护率均为100%;普克鲁胺可以加快病毒的清除,用药7天后病毒阳性转阴率为82%(安慰剂组为31%)。普克鲁胺在巴西的针对重症新冠患者的III期临床试验结果显示,普克鲁胺将重症新冠患者死亡风险降低了78%,入组至康复出院中位时间缩短了5天。
此外,2021年7月,普克鲁胺在巴拉圭获得首个紧急使用授权。
真实生物:阿兹夫定初步临床试验患者4天内首次核酸转阴率达90%
阿兹夫定由真实生物研发,是国产新冠病毒口服药物的代表性药物之一,目前正在中国、巴西、俄罗斯开展III期临床。同时,据公开资料显示,阿兹夫定也是全球首个双靶点抗艾滋病1类新药,曾获得中国专利金奖。
据真实生物公众号消息,早在2020年新冠疫情之初,阿兹夫定就开展了治疗COVID-19的相关探索,通报会上披露,初步临床试验中,10位患者4天内第一次核酸转阴率达到90%。
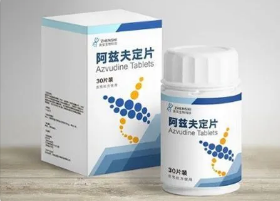
2021年12月,中国医科院蒋建东等研究显示,阿兹夫定(FNC)单磷酸盐类似物抑制SARS-CoV-2和HCoV-OC43冠状病毒;大鼠试验中FNC三磷酸(活性形式)集中在胸腺和外周血单核细胞中。一项随机单臂试验中,31名患者口服 FNC后在3.29~2.22天内全部实现病毒核糖核酸检测转阴;在9.00~4.93天内全部出院。
目前,阿兹夫定用于轻症新冠感染者的巴西Ⅲ期临床试验已于2021年7月完成,用于治疗中、重度新冠肺炎的巴西Ⅲ期临床试验正在进行中;中国临床试验注册中心数据则显示,2021年11月,郑州大学第一附属医院已注册了阿兹夫定开展针对Delta变异株的Ⅲ期临床试验。
【辉瑞新冠口服特效药获准进入中国】相关文章:
中国紧急获批辉瑞新冠口服药02-12
辉瑞新冠口服药药效如何02-12
辉瑞新冠口服药是哪个国家的02-12
辉瑞新冠口服药什么时候上市02-12
辉瑞新冠口服药获批进口注册02-12
中国批准辉瑞新冠治疗药物进口注册02-12
多款新冠口服药将在年内上市02-10
新冠疫情防控工作方案02-09
国产单针新冠疫苗量产上市01-28
孕期接种新冠疫苗婴儿将受益02-09